La química dels hidrocarburs s’estudia en els primers anys del grau de Química perquè és una de les que presenta unes regles més senzilles i més ben establertes. De fet les regles sobre la tetravalència del carboni i la formació de cadenes a través de la unió d’àtoms de C (enllaços C—C) en els hidrocarburs daten de l’any 1858 i es deuen a Kekulé i Archibal Scott Couper.
A la química del carboni ens trobem en la major part dels compostos amb els típics enllaços C-C i C-H localitzats de dos centres i dos electrons (2c-2e). La hibridació dels àtoms de C que pot ser sp3, sp2 i sp ens porta a enllaços amb angles de 109.5º i orientació tetraèdrica (3D), enllaços de 120º i estructures planes (2D) o enllaços de 180º i estructures lineals (1D).
La química dels hidrurs de bor és força més complicada. Els hidrurs de bor acostumen a evitar els enllaços B-B de 2c-2e i a diferència dels hidrocarburs és difícil trobar llargues cadenes de sistemes units a través d’enllaços B-B. Mentre en els hidrocarburs és molt excepcional una coordinació superior a 4, a la química del bor la coordinació de fins a 7 és habitual. Finalment, mentre en els hidrocarburs és fàcil trobar molècules amb enllaços dobles (etè) o triples (etí), a la química dels hidrurs de bor aquestes espècies són més aviat rares.
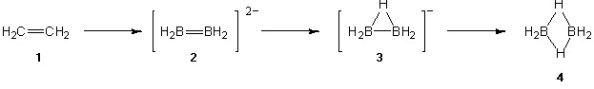
Doncs bé malgrat les diferències evidents entre les químiques dels hidrocarburs i dels hidrurs de bor, s’ha descrit recentment un procediment que permet a partir de qualsevol hidrocarbur generar hidrurs de bor anàlegs. El més senzill és explicar-ho a través d’un exemple. Considerem l’etè, 1 a la Figura 1. El podem transformar a un hidrur de bor canviant cada C per un B–. D’aquesta manera, l’hidrur de bor format 2 té els mateixos electrons de valència que l’etè de partida. A partir d’aquest compost podem afegir un protó (H+) per cada enllaç B-B de 2c-2e (en aquest cas particular tenim dos enllaços B-B, un σ i un π) que hi hagi en el nostre compost inicial. A l’afegir un protó es forma un enllaç B-H-B de 3c-2e que substitueix l’inicial B-B de 2c-2e i es redueix una càrrega negativa. Així, la primera substitució genera l’anió 3 que es pot considerar un anàleg de l’etè. Una segona substitució forma 4 que és la coneguda molècula de diborà. Una tercera substitució ja no és possible perquè no tenim cap més enllaç B-B de 2c-2e en el sistema 4. Les molècules 2, 3 i 4 són hidrurs de bor anàlegs de l’etè.
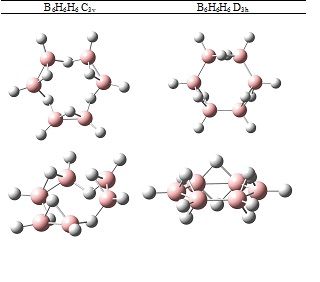
L’exercici que hem fet amb l’etè es pot repetir amb qualsevol molècula d’hidrocarbur (us animo a fer-ho) i descobrir els hidrurs de bor anàlegs a l’hidrocarbur inicial. D’aquesta manera es poden recuperar molts hidrurs de bor ja coneguts (com el diborà) i es poden proposar noves estructures com ara el compost 3 que possiblement seran sintetitzades en un laboratori en un futur no massa llunyà. Com a exemple, dir-vos que fent aquest experiment amb el benzè surten estructures com les de la Figura 2.
Tot aquest procediment ha estat elaborat per investigadors de l’Institut de Química Computacional i Catàlisi de la UdG en col·laboració amb investigadors de l’Institut de Ciència dels Materials (ICMAB) del CSIC. I ha estat recentment descrit en un article catalogat com a VIP (very interesting paper) per l’editor de Chemistry – A European Journal. Aquest article ha merescut la contraportada del número 19 de la revista (obra del Dr. Jordi Poater, Figura 3).







Posted on 29/03/2013 per miquelsola
0