Dedicat a totes les Carmes, Maria Carmes, Carmines i Carmetes
Vaig començar els estudis de Química l’any 1981 al Col·legi Universitari de Girona. Entre els nostres professors hi havia el Dr. Joan Miró que l’any 1982 (o 1983 potser?) va convidar al Prof. Joan Bertran de la UAB a donar-nos una conferència. El títol no el recordo exactament però crec que recordar que més o menys era una cosa com ara “Aigua, catalitzador bifuncional“. Al llarg de la seva xerrada el Prof. Bertran va destacar el paper del dissolvent, i en particular de l’aigua, en les reaccions químiques. Aquesta, de fet, ha estat una de les línies de recerca principals del Prof. Bertran que és des d’octubre de 2004 Doctor Honoris Causa per la Universitat de Girona. La conferència la recordo amb estima perquè va ser un dels primers cops que vaig sentir a parlar de la química computacional.
Com a catalitzador l’aigua pot tenir un efecte purament “físic” estabilitzant aquelles espècies que tenen una més gran separació de càrrega per efecte de la seva polaritat sense intervenir directament en el mecanisme de la reacció. Això és el que passa en el cas de la reacció de Menshutkin (Figura 1) que varem comentar en una entrada anterior. En la reacció de Menshutkin partim de dues espècies neutres i acabem amb dues espècies carregades. Al llarg de la coordenada de reacció es va produint la separació de càrrega i els dissolvents més polars (l’aigua entre ells) afavoreixen la reacció per pura interacció electrostàtica de la càrrega generada amb els dípols de l’aigua. La reacció, que és molt endotèrmica en fase gas, passa a ser exotèrmica en solució aquosa.
Hi ha reaccions, però, en les que l’aigua no té un paper d’espectador sinó que juga un rol més actiu i intervé directament en la reacció química. Hi ha molts d’exemples, però per il·lustrar-ho escolliré la reacció de transferència protònica que té lloc en l’anomenat mecanisme de Lipscomb que opera en l’enzim anhidrasa carbònica i que vàrem estudiar en el grup del Prof. Bertran l’any 1992. Aquest enzim catalitza la transformació del CO2 (diòxid de carboni) a HCO3– (bicarbonat) i ho fa a través de dos possibles mecanismes: el de Lipscomb i el de Linsdkog (veure Figura 2). En absència de molècules d’aigua el mecanisme de Lipscomb passa a través de l’estat de transició TS_(a) de la Figura 3 i no és competitiu amb el de Lindskog que té una barrera molt més baixa. Tanmateix, si la transferència protònica ve ajudada per una molècula d’aigua (TS_(b) de la Figura 3), la barrera del mecanisme de Lipscomb disminueix de manera molt substancial (i per tant l’aigua catalitza el procés) i passa a ser competitiu amb el mecanisme de Lindskog. La raó l’hem de buscar en el fet que la transferència protònica en el TS_(a) es fa a través d’un anell de 4 membres (O1H1O2C) que està molt tensionat, mentre que en el TS_(b) es genera un anell de 6 membres molt menys tensionat. En el TS_(b) l’aigua dóna un protó al CO2 i n’accepta un altre del grup L3ZnOH, és a dir, fa de catalitzador bifuncional (l’aigua actua com acceptora i donadora de protons en un procés simultani).

Figura 3. L’estat de transició del mecanisme de Lipscomb (a) sense aigua i (b) amb una molècula d’aigua.
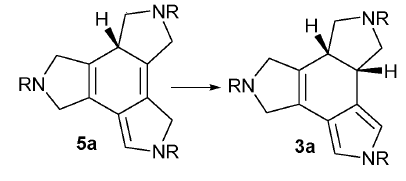
D’exemples on una molècula d’aigua explícita actua de catalitzador bifuncional ajudant a la transferència d’un protó n’hi ha molts. Menys freqüent és el cas on la molècula d’aigua fa el mateix paper però transferint un àtom d’hidrogen (un H· radical). L’any 2010 vàrem publicar un treball conjunt amb el grup de la Prof. Anna Roglans del grup de recerca METSO de la UdG en el que estudiàvem una reacció de cicloisomerització de dos triples enllaços i un enllaç doble per formar un anell de ciclohexadiè que no requeria la presència d’un catalitzador (a diferència del que passa normalment). En aquesta reacció hi havia una transferència 1,3 d’hidrogen (pas 5a a 3a en la Figura 4) que vàrem calcular que tenia una barrera molt alta. Després de provar diferents funcionals, bases de càlcul, etc. vàrem concloure que no era un problema del mètode de càlcul. Amb poca convicció vàrem provar la possibilitat que una molècula d’aigua actués com a catalitzador bifuncional, però ara per transferir un àtom d’hidrogen, no un protó. La barrera catalitzada per una molècula d’aigua va baixar més de 40 kcal/mol! L’estat de transició és el que es pot veure a la Figura 5. El resultat teòric es va poder confirmar experimentalment utilitzant aigua deuterada i veient que s’incorporava un àtom de deuteri en el producte final. A més cal tenir en compte que al fer-se la reacció a reflux és inevitable que hi hagi traces de molècules d’aigua a la reacció.
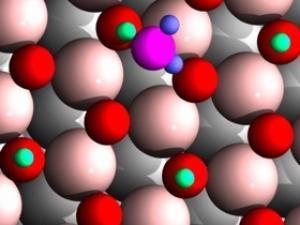
Finalment, aquest mes de maig de 2012 investigadors de les Universitat de Wisconsin i Florida han publicat un treball a Science on es demostra que la difusió d’àtoms d’hidrogen sobre la superfície d’òxid de ferro o titani s’accelera en presència de molècules d’aigua. La difusió d’hidrogen sobre les superfícies és important en reaccions d’hidrogenació, deshidrogenació i emmagatzematge d’hidrogen. A partir d’estudis teòrics i estudis d’efectes cinètics d’isòtop s’ha determinat que la presència d’aigua facilita la mobilitat dels àtoms d’hidrogen a través d’un estat de transició on es forma una espècie propera al H3O+ (veure Figura 6).
En definitiva, una molècula tan senzilla com la molècula d’aigua pot catalitzar un nombre molt gran de processos alguns d’ells d’importància industrial. La catàlisi pot ser exclusivament de tipus “físic” per estabilització de les espècies amb més separació de càrrega o “química” per intervenció directa d’una (o més d’una) molècula d’aigua en el mecanisme de reacció. En aquest darrer cas l’aigua opera com un catalitzador bifuncional.
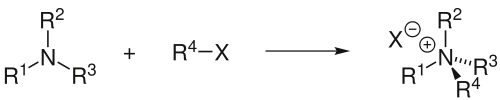








Posted on 16/07/2012 per miquelsola
0