La revista Chemical & Engineering News ha encetat un bloc durant l’Any Internacional de la Química en el que es pot fer una entrada describint la teva reacció preferida. Entre les reaccions descrites en aquest bloc hi podem trobar la reacció de cicloaddició Diels-Alder, les reaccions de combustió d’hidrocarburs, la reacció de Maillard tan important a la cuina, la reacció oscil·lant de Belousov-Zhabotinsky, la reacció de Grignard de la que vàrem parlar en aquest bloc, la reducció de Birch, la reacció d’esterificació, la reacció de metàtesi d’olefines, l’addició de Michael i unes quantes més. Totes elles reaccions molt importants en la història de la Química. Dins la llista de reaccions favorites però no hi ha la meva, que és l’anomenada reacció de Menshutkin i que aprofito ara per comentar-la.
La reacció de Menshutkin va ser descrita per primer cop l’any 1890 pel químic rus Nikolai Aleksandrovich Menshutkin en un article titulat “Über die Affinitätkoeffizienten der Alkylhaloide un der Amine”. Consisteix en l’alquilació d’amines terciàries per halogenurs d’alquil (Figura 2). La reacció de Menshutkin és un tipus especial de reacció SN2, en la que els reactius són tots dos neutres, en contrast amb la SN2 més habituals on un dels reactius està carregat. Concretament Menshutkin va estudiar la reacció entre la trietilamina i el iodur d’etil a 100 ºC en molts dissolvents de diferent polaritat. Per aquesta reacció Menshutkin va trobar que la velocitat de reacció augmenta considerablement amb la polaritat del dissolvent emprat, de manera que va arribar a la conclusió el medi de reacció tenia una gran influència en les reaccions químiques. Lamentablement, les profundes implicacions de aquest estudi pioner de Menshutkin van passar desapercebudes durant molts anys pels químics de l’època.
L’any 1991 varem estudiar aquesta reacció considerant el model NH3 + CH3Br → NH3CH3+ + Br– des d’un punt de vista teòric i vàrem obtenir els perfils de reacció que es mostren a la Figura 3. La reacció en fase gas és extraordinàriament endotèrmica. A mesura que augmenta la polaritat del solvent la reacció es va fent més exotèrmica i la barrera de la reacció també disminueix. No és d’estranyar aquest resultat perquè es tracta d’una reacció amb separació de càrregues, altament afavorida en dissolvents polars. No només això, sinó que també és molt interessant el fet que canvia substancialment la geometria de l’estat de transició que a mesura que augmenta la polaritat del solvent agafa una estructura més propera als reactius tal com prediu el postulat de Hammond.

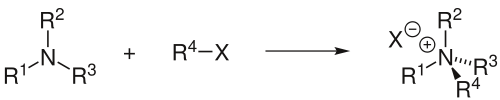







Juliol 16th, 2012 → 5:41 am
[…] sense intervenir directament en el mecanisme de la reacció. Això és el que passa en el cas de la reacció de Menshutkin (Figura 1) que varem comentar en una entrada anterior. En la reacció de Menshutkin partim de dues espècies neutres i acabem amb dues espècies […]